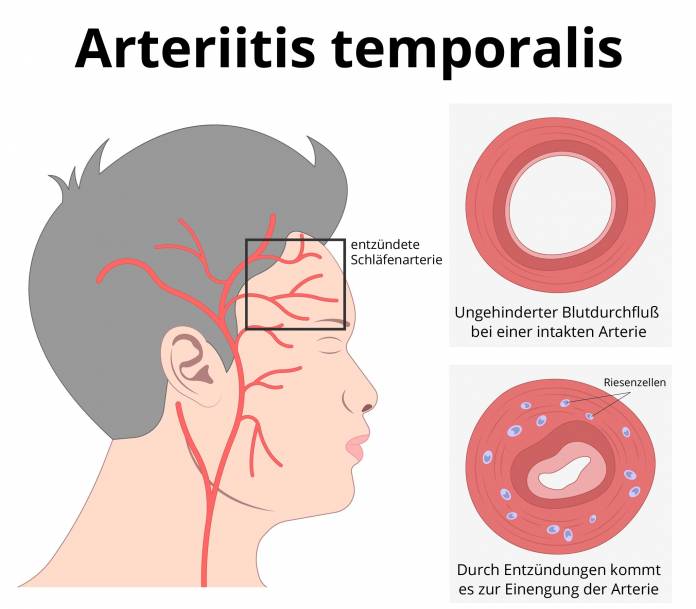
Arteriitis temporalis (Horton-Krankheit, Riesenzellarteriitis)
Die Arteriitis temporalis (Morbus Horton, Riesenzellarteriitis) ist eine spezielle Form einer Gefäßentzündung (Vaskulitis). Es handelt sich somit um eine entzündliche Erkrankung, bei der die Gefäßwände von Arterien im ganzen Körper betroffen sein können. Die Entzündungen treten meist im Bereich der Schädeldecke und des Kopfes auf. Die Beteiligung der Schläfenarterie (Arteria temporalis superficialis) ist zwar ein im Krankheitsgeschehen fulminantes Ereignis, tritt aber nicht zwingend bei einer Riesenzellarteriitis auf.
Betroffene leiden unter anhaltenden Kopfschmerzen, Gliederschmerzen und Fieber. Hinzu kommen Nachtschweiß und unfreiwilliger Gewichtsverlust. Sie äußerte sich sehr häufig durch Gefäßverschlüsse im Auge. Die Erkrankung kann dadurch innerhalb relativ kurzer Zeit zur Erblindung beider Augen führen. Deshalb sollte bei Verdacht auf eine solche Horton-Krankheit, insbesondere aber bei bestimmten Gefäßverschlüssen des Auges, eine Biopsie (Probeentnahme) der Schläfenarterie (Arteria temporalis) erfolgen, um die Krankheit nachzuweisen oder weitestgehend auszuschließen.
Diese Symptome sind Grund genug, dringend einen Arzt aufzusuchen. Wenn Menschen mit solchen Beschwerden über 50 Jahre alt sind, Kopfschmerzen im Bereich der Schläfen auftreten und sich bereits Sehstörungen zeigen, ist Eile geboten. Meist sind ältere Patienten betroffen, Frauen geringfügig häufiger als Männer.
Ursachen
Die Riesenzellarteriitis zählt zu den Autoimmunerkrankungen: Ein Mechanismus sorgt dafür, dass sich unser Immunsystem gegen körpereigene Zellen richtet. Im Falle der Riesenzellarteriitis ist es das Endothel (die innerste Schicht) von Arterien, welches angegriffen wird.
Es gibt Hinweise für ein Ansteigen der Krankheitshäufigkeit nach dem 50. Lebensjahr sowie Anzeichen für ein Nord-Süd-Gefälle in Deutschland. Eine exakte Aussage über mögliche Ursachen der Riesenzellarteriitis lässt sich aktuell jedoch nicht geben.
Einflüsse wie Umweltfaktoren oder das Vorliegen einer genetischen Disposition (Veranlagung) spielen eine entscheidende Rolle. Diskutiert wird auch ein Zusammenhang mit dem Forestier-Certonciny-Syndrom, einer nicht entzündlichen Skeletterkrankung. Unabhängig aller potenziellen Ursachen scheint eine gesunde Ernährung und ein ausgeglichener Lebensstil einen vorbeugenden Einfluss auf die Riesenzellarteriitis auszuüben.
Im Jahr 1932 hat der amerikanische Arzt B.T. Horton die Riesenzellarteriitis, die auch Morbus Horton genannt wird, durch feingewebliche Untersuchungen (histologisch) gesichert. Er erkannte, dass es sich um Entzündungen an der Innenwand der Arterien handelt. An diesem Geschehen sind vorwiegend T-Lymphozyten und Makrophagen beteiligt. Makrophagen werden auch als Fresszellen bezeichnet und sind ein wichtiger Bestandteil des Entzündungsprozesses. Bei jeder Entzündung werden körperfremde Substanzen vom Immunsystem erkannt und mittels der Fresszellen vernichtet. Im Falle der Riesenzellarteriitis werden die T-Zellen durch eine Fehlsteuerung unseres Immunsystems verändert. Diese richten sich nun auch gegen die körpereigenen Zellen in den Gefäßen. Es entsteht eine Entzündung, in deren Verlauf die Fresszellen zu Riesenzellen verschmelzen. Die entzündlichen Prozesse führen zu einer Einengung des inneren Durchmessers (Lumen) der Arterien und schließlich zu einer Minderdurchblutung der entsprechenden Organe. Die Veränderungen der Gefäßwand können zudem zur Ausbildung von Aneurysmen führen. Dies sind Ausstülpungen der Arterien, die dringend einer Behandlung bedürfen. Das Vorhandensein von Aneurysmen ist ein lebensbedrohlicher Zustand, da sie entweder platzen können oder die Bildung von Blutgerinnseln in der Aussackung verursachen können.
Neuere Forschungen berichten von einem möglichen Zusammenhang mit Hepatitis-B-Viren, Influenzaviren (Grippeviren) oder Varizella-Zoster-Viren (Erreger der Windpocken und Gürtelrose). Auch Bakterien wie Borrelien könnten einen Krankheitsausbruch hervorrufen.
Symptome
Erste Anzeichen äußern sich in starken, anhaltenden Kopfschmerzen und Beschwerden im Bereich der Kiefermuskulatur. Werden diese nicht erkannt und sofort behandelt, können sie zu Blindheit oder anderen tiefgreifenden Komplikationen führen. Grundsätzlich kann man die Symptome einer Riesenzellarteriitis in vier Kategorien einteilen:
- Beteiligung kranieller Gefäße (Kopf)
- Beteiligung großer Gefäße
- Systemische (allgemeine) Entzündungszeichen
- Polymyalgia rheumatica (Krankheitsbild mit Muskelschmerzen)
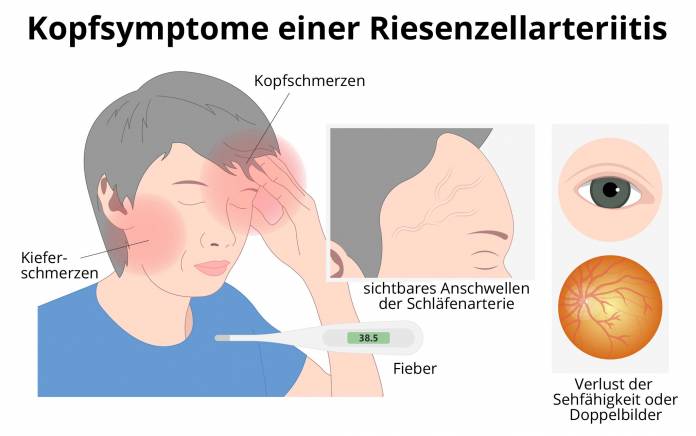
Kopfsymptome
Drei Viertel aller an der Riesenzellarteriitis erkrankten Patienten berichten über Kopfschmerzen. In diesen Fällen treten die oft langanhaltenden Schmerzen beidseits an den Schläfen auf. Die Schläfenarterie kann deutlich sichtbar anschwellen und pochend schmerzhaft sein. Die Arterie kann verhärtet sein und nicht mehr pulsieren. Eine Behandlung mit den üblichen Analgetika (Schmerzmitteln) ist nicht zielführend (analgetikarefraktär).
Beschwerden beim Kauen (Kauclaudicatio) oder Schlucken (Schluckclaudicatio) können durch eine Minderdurchblutung der Kaumuskulatur oder der Zunge auftreten. Umgangssprachlich wird diese Symptomatik auch Kieferhinken genannt. Die Erkrankten klagen über eine überempfindliche Kopfhaut. Aufgrund dieses Scalp-Tenderness-Syndroms empfinden Patienten ihre Kopfhaut als extrem sensibel. Selbst das Haarekämmen kann Schmerzen verursachen.
Weitaus dramatischer ist der plötzliche und schmerzlose Verlust der Sehfähigkeit. Das kann sich sowohl in einer Abnahme der Sehschärfe als auch in Doppelbildern (Diplopie) ausdrücken. Bei der sogenannten stillen Form der Riesenzellarteriitis ist die spontane Erblindung, meist eines Auges, das erste Symptom überhaupt. Ohne eine rasch eingeleitete Therapie führt dies bei bis zu 60 Prozent der Erkrankten zum Verlust der Sehschärfe des zweiten Auges. Die Ursache der Doppelbilder findet man in einer Ischämie (Minderdurchblutung) der Augenmuskulatur oder auch des Hirnstammes, während Mikroinfarkte (sogenannte cotton wool spots) der Netzhautnerven für die Abnahme an Sehschärfe verantwortlich gemacht werden.
In den meisten Fällen ist ein Auge, nicht selten aber auch beide Augen von den Folgen der Horton-Erkrankung betroffen. Es kann sich ein Arterienverschluss mit Durchblutungseinschränkung des Sehnervenkopfes (anteriore ischämische Optikusneuropathie) entwickeln. Seltener tritt auch ein Verschluss der zentralen Netzhautarterie (Zentralarterienverschluss, ZAV) auf. In beiden Fällen kommt es zu einer plötzlichen starken Sehverschlechterung, die zur Erblindung des betroffenen Auges führen kann. Innerhalb kurzer Zeit kann sich ebenfalls eine Erblindung des anderen Auges ergeben. Auch lebensgefährliche Komplikationen der Horton-Krankheit sind prinzipiell möglich, unter anderem Arterienverschlüsse im Gehirn.
Bei etwa 25 Prozent der an Morbus Horton erkrankten Patienten entwickelt sich im Krankheitsverlauf eine Polyneuropathie. So kommt es zusätzlich zu neurologischen Schmerzzuständen im betroffenen Bereich.
Beteiligung großer Gefäße
Bei der Mehrheit der Patienten mit Riesenzellarteriitis findet sich in bildgebenden Verfahren eine Beteiligung der Aorta, also der Hauptschlagader. Ebenso können die großen Arterien, welche der Versorgung von Kopf (Arteria subclavia), Herz (Arteria coronaria) oder anderen großen Organen dienen, betroffen sein. Bedenklich ist diese Situation, da man davon ausgeht, dass bei 20 Prozent aller Erkrankten Aneurysmen (Gefäßaussackungen) auftreten. So sind Aneurysmen der Aorta im Brustbereich um den Faktor 17 häufiger, als dies bei der normalen Bevölkerung der Fall ist. Ebenso steigt das Risiko, einen Schlaganfall oder einen Herzinfarkt zu erleiden.
Die Patienten berichten über unspezifische Schmerzen im Bauchraum oder Brustbereich. Bei Bauchschmerzen handelt es sich meist nur um Begleitsymptome, die zum Beispiel durch Verstopfung hervorgerufen werden. In seltenen Fällen tritt aber auch eine sogenannte mesenteriale Riesenzellarteriitis auf, die bei einem Drittel der davon betroffenen Patienten zum Tod führen kann.
Brustschmerzen können durch eine ganze Reihe unterschiedlicher Symptome gekennzeichnet sein.
Systemische Entzündungszeichen
Allgemeines Krankheitsempfinden ist ein vor allem im Alter häufiges Beschwerdebild. Genauer finden sich Symptome wie Fieber, Nachtschweiß, ungewollter Gewichtsverlust, Bauch- oder Kopfschmerzen. Das individuelle Schmerzempfinden ist unterschiedlich stark ausgeprägt. Beim Erscheinen mehrerer der genannten Symptome ist ein Arztbesuch jedoch dringend angeraten. Gerade bei einer ausschließlichen Beteiligung der großen Arterien, ohne symptomatische Durchblutungsstörungen, ist dieses allgemeine Krankheitsempfinden oft der einzige Hinweis auf eine mögliche Riesenzellarteriitis.
Polymyalgia rheumatica
Das Auftreten der Riesenzellarteriitis ist in beinahe der Hälfte aller Fälle mit der als Muskelrheuma bekannten Polymyalgia rheumatica vergesellschaftet. Charakteristisch für eine Beteiligung der Polymyalgia rheumatica sind Muskelschmerzen im Rumpfbereich. Gerade nachts treten sehr starke Schmerzen im Schultergürtel und der Hüfte auf. Einhergehend mit dem Schmerz kann es zu einem Schwächegefühl oder einer Druckempfindlichkeit vor allem der Arme kommen. Als Ursache kommt hier eine entzündliche Autoimmunreaktion der bindegeweblichen Anteile der Gelenke infrage.
Diagnose
Die Diagnose der Riesenzellarteriitis erfolgt durch das Zusammenwirken klinischer Beurteilung, bildgebender Verfahren, einer gezielten Labordiagnostik sowie der mikroskopischen (pathohistologischen) Bewertung des Gewebes. Eine wichtige Hilfestellung sind hierbei die vom American College of Rheumatology (ACR) herausgegebenen Kriterien. Diese sollen vor allem der Unterscheidung zu anderen entzündlichen Gefäßveränderungen (Vaskulitiden) dienen. Ein möglichst rascher Nachweis der Erkrankung wird insbesondere angestrebt, da mit schwersten bis tödlichen Verläufen zu rechnen ist. Eine Diagnose kann häufig auch ohne MRT oder histologischen Verfahren, durch den Einsatz einer Duplexsonografie (spezielle Ultraschalluntersuchung) erreicht werden. Die bloße Verbesserung der Symptome durch eine Ersttherapie ist nicht beweisend für eine Riesenzellarteriitis.
ACR-Kriterien
Das American College of Rheumatology hat sowohl für die Riesenzellarteriitis als auch für die Polymyalgia rheumatica einen Kriterienkatalog vorgelegt. Dieser dient einerseits der Unterscheidung beider Erkrankungen, gleichermaßen soll er eine standardisierte Verlaufskontrolle ermöglichen. Das Zustandekommen von wenigstens drei der unten aufgeführten fünf Kriterien kann zu einer Sicherstellung der Diagnose Riesenzellarteriitis führen. Der Test verfügt schon bei drei Fünftel aller Anhaltspunkte über eine Sensitivität (Erkennungsrate) von größer als 92 Prozent. So ist eine sehr hohe Treffsicherheit bei der Diagnostik gewährleistet. Die ACR-Kriterien sind:
- Alter über 50 Jahre
- neu aufgetretene Kopfschmerzen
- auffällige Temporalarterien (Schläfenarterien mit Pulslosigkeit, Verhärtung, Druckschmerz, Schwellung)
- BSG (Blutsenkungsgeschwindigkeit) > 50 mm in der ersten Stunde
- auffällige Biopsie (Gewebeprobe) der Temporalarterie
Klinik
Eine ausführliche Anamnese (Arzt-Patienten-Gespräch) kann erste wichtige Hinweise liefern. So können die Art und das Auftreten eines Kopfschmerzes erfragt werden. Auch die Information über eine möglicherweise erfolgte eigene Medikamenteneinnahme kann bei dem hier typischen analgetikarefraktären (nicht auf Schmerzmittel ansprechenden) Kopfschmerz wichtig sein.
Die Palpation (Abtasten) der Schläfenarterien ist vor allem im Hinblick auf die Häufigkeit und Schwere einer Augenbeteiligung wichtig. Im Krankheitsfall kann sich die Temporalarterie abnormal verdickt anfühlen und sich bei Druck aufrollen, anstatt zu kollabieren.
Schmerzen im Bereich des Kiefergelenkes mit deutlichen Kau- und Schluckbeschwerden werden mit Sicherheit vom Patienten erkannt. Damit wären schon drei der relevanten ACR-Kriterien erfüllt.
In den Bereich der klinischen Untersuchung gehört schon bei einem Anfangsverdacht eine augenärztliche Untersuchung. Der Verdacht auf eine Riesenzellarteriitis ist ein augenärztlicher Notfall. Wenn die Sehkraft bei der Riesenzellarteriitis nachlässt, geschieht dies schlagartig, jedoch meist schmerzlos. Ursächlich ist ein teilweiser oder vollständiger Gefäßverschluss der Netzhaut oder eine verminderte Blutzufuhr des Sehnervs. Ein Hinweis des Patienten auf Doppelbilder oder stark eingeschränkte Sehkraft bedarf einer sofortigen notfallmäßigen Behandlung.
Labor
Die wichtigsten Laborparameter, welche zur Diagnostik der Riesenzellarteriitis herangezogen werden, sind die Blutsenkungsgeschwindigkeit (BSG) sowie das C-reaktive Protein (CRP). Bei beiden Laborparametern handelt es sich um nicht sehr spezifische Methoden. Gemeinsam mit einem positiven Symptombefund lässt sich die Diagnose Riesenzellarteriitis jedoch mit großer Sicherheit feststellen.
Bei der Blutsenkungsgeschwindigkeit lassen vor allem Werte von 90 mm nach der ersten Stunde aufhorchen. Man spricht bei dieser stark beschleunigten Blutsenkung von einer Sturzsenkung, die eine gewisse unterscheidende (differenzialdiagnostische) Bedeutung aufweist. Im Anfangsstadium des Morbus Horton kann eine Blutsenkungsgeschwindigkeit jedoch auch normwertig sein.
Als sogenanntes Akut-Phase-Protein ist das C-reaktive Protein (CRP) ebenfalls ein wichtiger Entzündungsmarker in der Routinediagnostik. Das C-reaktive Protein setzt wichtige zelluläre Abwehrmechanismen unseres Immunsystems in Gang. Es besitzt die Fähigkeit, sich an Bakterien und defekte Zellen anzuheften. Auf diese Weise können diese von den Fresszellen erkannt werden. Mit Werten von 9 mg/l gilt dieser Parameter als deutlich erhöht. Das C-reaktive Protein normalisiert sich innerhalb einer Woche bei einer Behandlung mit Steroiden (Cortison). So kann das C-reaktive Protein auch als anfängliche Verlaufskontrolle bei der Therapie herangezogen werden.
Nur ein sehr geringer Anteil der Patienten mit Riesenzellarteriitis zeigt keine serologisch nachweisbaren Entzündungszeichen. Besonders fatal ist dies, wenn auch keine typischen klinischen Anzeichen auf die Erkrankung hindeuten. Bei dieser sogenannten stillen Form der Riesenzellarteriitis kommt es ohne Vorwarnung zum plötzlichen Sehverlust.
Die Sicherung der Diagnose erfolgt in solchen Fällen durch weitere Laboruntersuchungen, die jedoch eine verhältnismäßig geringe Spezifität aufweisen. Im Blutbild können sich Veränderungen finden (eine normochrome normozytäre Anämie, auch eine mäßige Leukozytose und Thrombozytose sind möglich). Der Nachweis von speziellen Antikörpern (Auto-Antikörper gegen Ferritin) gelingt bei fast allen unbehandelten Patienten. Allerdings werden diese Antikörper auch bei anderen autoimmunen Krankheiten des rheumatischen Formenkreises nachgewiesen.
Bildgebende Verfahren
Unter den bildgebenden Verfahren, die zur Darstellung von Gefäßen zur Verfügung stehen, ist die Duplexsonografie die beste. Diese Variante der Ultraschalluntersuchung gibt dem Arzt schnell ein umfassendes Bild des Krankheitsgeschehens. Für den Patienten ist die Untersuchung schmerzfrei. Da weder Strahlungen auftreten noch ein Kontrastmittel verabreicht wird, ist es zudem frei von Risiken. Die Duplexsonografie kombiniert das Bild einer normalen Ultraschalluntersuchung mit der Dopplersonografie, bei welcher der Blutfluss farbig dargestellt werden kann. Diese beiden Bilder liegen übereinander und sind zudem in der Lage, den Zustand der Gefäßwand aufzeigen sowie die Fließgeschwindigkeit des Blutes zu errechnen. Mit diesem Verfahren kann der Arzt drei Fragestellungen klären, die zur Diagnostik des Morbus Horton wichtig sind:
- Vorhandensein eines entzündlichen Gefäßödems (Wassereinlagerung), das sogenannte Halo-Phänomen
- Stenosen (Verengungen)
- akuter entzündlicher Verschluss
Mit der Duplexsonografie können auf diese Weise andere Untersuchungsmethoden wie Biopsie oder MRT umgangen werden.
Biopsie der Schläfenarterie, Histologie
Obgleich die Diagnose einer Riesenzellarteriitis durch die bisher beschrieben Verfahren als gesichert erscheint, kann dennoch die Biopsie der Schläfenarterie empfehlenswert sein. Hierfür wird, meist aus der Schläfenarterie, ein etwa fünf cm langer Teil herausgenommen (reseziert). Da entzündliche Anteile im Gefäß nicht gleichmäßig verteilt sind, ist diese Länge empfehlenswert, um eine höhere Treffsicherheit zu erlangen.
In der feingeweblichen Aufarbeitung des Gewebeschnittes zeigt sich eine Entzündung der mittleren Wandschicht der Arterie (Tunica media). Dies geht mit einer knötchenhaften Ansammlung von Fresszellen, den sogenannten Granulomen, einher. Auch die äußere Hülle der Arterien (Tunica adventitia) zeigt entzündliche Prozesse. Diese Schicht ist mit dem umgebendem Bindegewebe verbunden. Das erklärt auch den ungewöhnlichen Tastbefund der Schläfenarterie. Zwischen der inneren (Tunica intima) und mittleren (Tunica media) Wand der Arterien lassen sich die namensgebenden Riesenzellen finden.
Diese histologische Befundsicherung gilt als goldener Standard bei der Diagnostik der Riesenzellarteriitis. Da eine Minderdurchblutung des Auges binnen kurzer Zeit zu massiven Sehstörungen führen kann, wird für den Beginn einer Therapie die Biopsie nicht abgewartet. Entzündungssymptome klingen erst über einen längeren Zeitraum ab, sodass eine Gewebeprobe durchaus innerhalb von zwei Wochen nach Therapiestart durchgeführt werden kann.
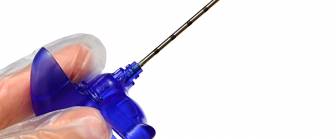
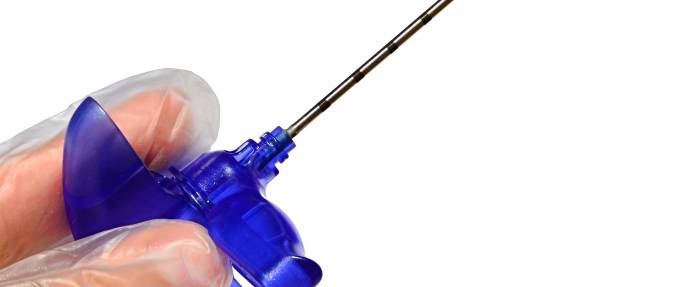
Durchführung der Biopsie der Schläfenarterie
Die Probeentnahme der Schläfenarterie (Arteria-temporalis-Biopsie) erfolgt in örtlicher Betäubung.
Die Haut der Schläfe über der Arterie wird eingeschnitten und das Gefäß freipräpariert. Die Arterie muss unterbunden werden. Daraufhin wird ein Abschnitt herausgeschnitten. Am Ende des Eingriffs wird die Haut wieder vernäht. Ein Verband wird angelegt.
Das entnommene Arterienstück wird zu einer feingeweblichen Untersuchung (Histologie) eingeschickt. Im Labor wird damit beurteilt, ob eine Arteriitis temporalis vorliegt oder nicht.
Komplikationen einer Biopsie der Schläfenarterie
Bei dem Eingriff kann es zu starken Blutungen, Nachblutungen sowie Blutergüssen kommen. Strukturen im Operationsbereich können verletzt werden. Nervenverletzungen können zu Lähmungserscheinungen oder Taubheitsgefühl führen. Durch die Gefäßabklemmung und -durchtrennung kann es bei Normvarianten der Durchblutung äußerst selten zur Minderversorgung des Auges und weiteren Gewebes kommen. Infektionen, Wundheilungsstörungen sowie überschießende Narbenbildung können vorkommen. Allergien können nicht ausgeschlossen werden.
Differenzialdiagnose
Gerade das zu Beginn oft unklare Beschwerdebild bedarf einer eindeutigen Abgrenzung der Riesenzellarteriitis zu ähnlich gelagerten Erkrankungen. Kopfschmerz und allgemeine Krankheitszeichen führen meist zum Allgemeinarzt als ersten Ansprechpartner. Eine ausführliche Befragung durch den Arzt und gewissenhafte Antworten vonseiten des Patienten können bei der möglichen Diagnose Morbus Horton entscheidende Faktoren für eine frühzeitige Therapie sein.
Aufgabe des Arztes ist es, zu beurteilen, wie spezifisch die genannten Symptome für eine Riesenzellarteriitis sind oder ob eine andere Erkrankung mit ähnlichem Beschwerdebild vorliegen könnte.
Erkrankungen des rheumatischen Formenkreises mit Gefäßentzündung stehen mit an erster Stelle einer Differenzialdiagnostik. Bei Patienten jenseits der 50 Jahre kommt die Polymyalgia rheumatica in Betracht. Diese geht bei etwa der Hälfte der an Riesenzellarteriitis erkrankten Personen mit einher. Bei der Polymyalgia rheumatica dominieren akut aufgetretene Schmerzen im Schultergürtel und der Hüfte. Im Labor sind die üblichen Entzündungsparameter, ähnlich der Riesenzellarteriitis, erhöht. Eine Hilfestellung bei der Unterscheidung können die von der Europäischen Liga gegen Rheuma (EULAR) und der amerikanischen Rheumatologengesellschaft (ACR) aufgestellten Kriterien sein. Histologisch lassen sich bei der der Polymyalgia rheumatica zusätzlich Entzündungszeichen in den großen Gelenken wie Hüfte, Schulter oder Nacken finden.
Als weitere Differenzialdiagnosen können die rheumatoide Arthritis (Gelenkrheuma) oder die Polymyositis (eine Muskelentzündung) aufgeführt werden. Die Beteiligung der Schläfenarterie ist zwar bei der Diagnose einer Riesenzellarteriitis entscheidend, kann aber auch bei einer Reihe weiterer Gefäßentzündungen (Vaskulitiden) wie Morbus Wegener auftreten.
Von den genauen Beschwerden des Patienten hängt es ab, welche weiteren Diagnosen möglich sind.
Kopfschmerzen
Kopfschmerzen können sich in über 200 verschiedenen Formen ausdrücken. Bei der Riesenzellarteriitis handelt es sich um symptomatische Kopfschmerzen, bei denen Veränderungen der Gefäße ursächlich sind. Wichtig ist der Schmerzcharakter. Das Schmerzempfinden ist individuell und kann auch von Tag zu Tag unterschiedlich wahrgenommen werden. Eine Hilfe zur Einordnung der Kopfschmerzen kann ein Kopfschmerzfragebogen sein.
Brustschmerzen
Ähnlich wie beim Kopfschmerz besitzen auch Schmerzen im Brustbereich ein breit gefächertes Spektrum an möglichen Ursachen. In erster Linie ist an Herz- oder Lungenerkrankungen als Auslöser zu denken. Gerade Brustschmerzen sind oft angstbesetzt und bedürfen einer raschen Diagnose. Als primär ursächlich können hier Formen der Angina Pectoris, ein Herzinfarkt oder die Lungenembolie (Verschluss eines Lungengefäßes) benannt werden. Die entzündlichen Prozesse bei der Riesenzellarteriitis führen oft zu einer Durchblutungsstörung (Ischämie) und können eine ähnliche Symptomatik besitzen. Dem Arzt steht eine Reihe von Untersuchungsverfahren zur Verfügung, um diese abzugrenzen.
Beschwerden im Magen-Darm-Bereich
Hier kommen verschiedene Erkrankungen in Frage. Unter Medizinern hat die akute Mesenterialischämie einen traurigen Bekanntheitsgrad. Sie geht mit einer der höchsten Sterblichkeitsraten innerhalb der chirurgischen Intensivmedizin einher. Dies abzugrenzen ist ein Muss, da im Fall einer falschen Behandlung ein Darminfarkt zu erwarten ist.
Fieber unklarer Genese
Wenn außer den für Fieber typischen Zeichen keine weiteren Symptome vorhanden sind, lautet die Diagnose oft Fieber unklarer Genese. Gerade wenn sich die Entzündung ausschließlich auf die großen Arterien und die Aorta beschränkt, könnte es sich hier um Morbus Horton handeln.
Amaurosis fugax
Amaurosis fugax bezeichnet eine meist nur wenige Augenblicke andauernde, flüchtige Blindheit. Dieses plötzliche und schmerzlose Auftreten dieser Symptomatik lässt an die fatalen Folgen einer Durchblutungsstörung aufgrund einer Riesenzellarteriitis denken. In diesem Fall ist vielfach der Verschluss der Hauptarterie der Netzhaut die Ursache. Verharmlosen sollte man dieses Phänomen nicht, da es sich durchaus um die Vorboten eines Schlaganfalles handeln könnte.
Polyneuropathie
Bei etwa einem Viertel der an Morbus Horton erkrankten Patienten entwickelt sich im Krankheitsverlauf eine Polyneuropathie, eine allgemeine Störung, von der mehrere Nerven betroffen sind. Die Polyneuropathie kann verschiedene andere Ursachen haben.
Behandlung
Sobald ein starker Verdacht auf die Erkrankung besteht, muss unverzüglich mit der Therapie begonnen werden. In der Vergangenheit hat die Forschung eine Behandlung von Entzündungen durch Steroide (Cortison-Präparate) kontinuierlich verbessern können. Die Behandlungserfolge waren bahnbrechend. Hoch dosierte Gaben dieser Medikamentengruppe (Steroide, Cortison) haben zu einer Besserung der Schmerzen geführt. Vor allem die Fähigkeit, die gefürchtete Erblindung aufzuhalten, haben dieser Therapie vorerst zum Durchbruch geholfen.
Eine Steroidtherapie birgt allerdings auch eine ganze Reihe von Nachteilen. Für jeden Patienten muss ein individuell abgestimmter Therapieplan erstellt werden. Die Gefahr eines Rezidivs (erneutes Auftreten der Erkrankung) ist bei bis zu 50 Prozent hoch. Außerdem muss mit einer Vielzahl von Nebenwirkungen gerechnet werden. Neben dem bekannten Halbmondgesicht kann es zu Sehstörungen durch den Grauen Star oder Grünen Star kommen. Störungen im Stoffwechsel wie Diabetes oder Osteoporose sind ebenso gefürchtete Nebenwirkungen. Eine Hemmung der Immunantwort (Immunsuppression) kann zwar erwünscht sein, führt aber auch zu einer verstärkten Infektanfälligkeit. Ferner können Veränderungen im psychischen Erleben auftreten. Um einerseits die Dosis der Cortisongaben zu verringern und anderseits die möglichen Nebenwirkungen auf niedrigem Niveau zu halten, gehen Wissenschaftler verstärkt den Weg, Kombinationstherapien zu erforschen.
Eine besondere Bedeutung bekommen hierbei spezifische (monoklonale) Antikörper gegen den Interleukin-6-Rezeptor. Interleukin 6 ist ein entscheidender Faktor bei der Entstehung der Riesenzellarteriitis. Ähnlich wie beim Cortison handelt es sich bei diesem Antikörper-Präparat um ein immunschwächendes Mittel (Immunsuppressivum), sodass Nebenwirkungen nicht ausbleiben. Aktuell kann dieser monoklonale Antikörper die Dosierung von Cortison um die Hälfte reduzieren. Weitere Vorteile sind eine deutlich geringere Rückfallrate bei gleichzeitig weniger dramatischen Nebenwirkungen. Noch laufen Studien, ob und in welchem Umfang das neue Medikament Cortison ersetzen kann.
Prognose
Vereinzelt gibt es die Aussage, die Riesenzellarteriitis sei bei einer frühzeitigen Erkennung heilbar. Sofern Heilung als Wiederherstellung der Ausgangssituation ohne erneutes Auftreten verstanden wird, ist man von einer Realisierung derzeit jedoch noch ein Stück weit entfernt. Durch die Cortisongabe kann in den meisten Fällen das Krankheitsgeschehen nach sechs Monaten bis zwei Jahren erfolgreich unterdrückt werden. Ein erneutes Auftreten (Rezidiv) kann vorkommen, ist allerdings selten.
Die Entstehung der Riesenzellarteriitis ist längst nicht vollständig erklärt. Es ist Aufgabe der Forscher, in fachübergreifenden Arbeitsgruppen herauszufinden, wie sich die beteiligten Immunzellen und Substanzen (Zytokine) innerhalb biochemischer Reaktionswege verhalten.
Hinweise zur Biopsie
Vor der Operation zur Biopsie (Gewebeentnahme)
Oftmals müssen Arzneimittel, die die Blutgerinnung negativ beeinflussen, in Absprache mit dem Arzt abgesetzt werden. Dies kann unter anderem Aspirin® und Marcumar® betreffen.
Nach der Operation
Falls die Operation ambulant vorgenommen wurde, muss sich der Patient abholen lassen, da er für24 Stunden kein Auto mehr fahren darf, außerdem dürfen keine Maschinen bedient werden und keine bedeutsamen Entscheidungen getroffen werden.
Das Ergebnis der feingeweblichen Untersuchung der Arteria temporalis steht meist nach einem bis mehreren Tagen fest. Bei hochgradigem Verdacht wird bereits vor Vorliegen des Resultates eine Cortison-Behandlung notwendig.
Sollten sich Auffälligkeiten ergeben, die auf Komplikationen hindeuten könnten, so sollte rasch der Arzt verständigt werden.
aktualisiert am 13.10.2022